Рассылка
Будьте в курсе последних обновлений – подпишитесь на рассылку материалов на Ваш e-mail
Подписаться-
Когнітивні порушення судинного генезу: діагностування, профілактика та лікування
-
Лікування ажитації за деменції, спричиненої хворобою Альцгеймера
-
Постінсультні нейропсихіатричні ускладнення: типи, патогенез і терапевтичні втручання
-
Перспективи застосування препаратів на основі рослинних компонентів для лікування депресії
-
Застосування диклофенаку за неврологічних станів: перевірена ефективність і пошук нових підходів
-
Постінсультний емоціоналізм: патофізіологія, поширеність та лікування
Лікування ажитації за деменції, спричиненої хворобою Альцгеймера
Зміст статті:
- Матеріали та методи дослідження
- Оцінювання результатів
- Результати дослідження
- Обговорення
- Висновки
Ажитація — стан збудження й неспокою — є поширеним симптомом в пацієнтів із деменцією, що спричиняє порушення когнітивних функцій і повсякденної активності, збільшує навантаження на доглядальників. До вашої уваги представлено огляд статті Y. Nakamura et al. «Brexpiprazole treatment for agitation in Alzheimer’s dementia: A randomized study» видання Alzheimers Dement (2024 Nov; 20 [11]: 8002–8011), у якій оцінювали ефективність фармакотерапії атиповим антипсихотиком у пацієнтів з ажитацією, що була спричинена деменцією за хвороби Альцгеймера.
Ажитація є поширеним нейропсихіатричним симптомом, який розвивається у 45 % пацієнтів із хворобою Альцгеймера (ХА) / деменцією (Halpern etal., 2019). Симптомам ажитації притаманні надмірна рухова активність, словесна або фізична агресія (Sano etal., 2024). Як відомо, ажитація пов’язана зі зниженням когнітивних функцій, порушенням повсякденної активності, збільшенням тяжкості деменції та підвищенням смертності (Scarmeas etal., 2007; D’Onofrio etal., 2012; Peters etal., 2015). Вона збільшує тягар для осіб, які здійснюють догляд пацієнтів з ажитацією, та для системи охорони здоров’я (Morris etal., 2015; Knapp etal., 2016; Cheng, 2017; Hiyoshi-Taniguchi etal., 2018). За прогностичними даними, у Японії (одній із країн із найвиразнішим старінням населення) поширеність деменції серед осіб віком ≥ 65 років до 2045 року перевищить 25 % (Nakahori etal., 2021). Очікується, що до середини століття кількість пацієнтів із деменцією, спричиненою ХА, у США зросте більш ніж удвічі, переважно через старіння представників покоління «бебі-бумерів» (Alzheimer’s Association, 2018).
Тож, якщо до 2050 року поширеність синдрому стійкого порушення когнітивних функцій внаслідок органічного ураження мозку в усьому світі зросте більш ніж удвічі, то й поширеність ажитації при деменції за ХА значно підвищиться.
Першим і єдиним препаратом для лікування ажитації за деменції, спричиненої ХА, став брекспіпразол, схвалений Управлінням із контролю за якістю харчових продуктів і лікарських засобів США (FDA, 2023). Хоча в багатьох країнах світу досі немає офіційно схвалених препаратів для лікування ажитації в осіб із ХА, що призводить до використання поза затвердженими показаннями засобів з обмеженою доказовою підтримкою, попри несприятливе співвідношення ймовірної користі й ризику (Antonsdottir etal., 2015; Aigbogun etal., 2020). Ажитація за деменції, спричиненої ХА, пов’язана з ураженням важливих ділянок мозку, зокрема лобової кори та мигдалини, у поєднанні з дисфункцією серотонінергічної системи, відносним збереженням активності дофамінергічної системи та гіперреактивністю норадренергічних нейронів (Rosenberg etal., 2015; Liu etal., 2018).
Брекспіпразол діє як частковий агоніст серотонінових 5-HT1A- і дофамінових D2-рецепторів, а також як антагоніст серотонінових 5-HT2A і норадреналінових α1B- / α2C-рецепторів (Maeda etal., 2014). Детальний механізм дії брекспіпразолу не з’ясовано, прогнозованим результатом такого комплексного впливу є зменшення ознак ажитації.
Натепер здійснено три міжнародні дослідження за участю пацієнтів з ажитацією, спричиненою деменцією за ХА, основним кінцевим результатом яких була зміна загального показника за опитувальником Когена–Мансфілда для оцінювання ажитації (CMAI) від вихідного рівня до 12-го тижня лікування (Grossberg etal., 2020; Lee etal., 2023). У першому дослідженні застосовували фіксовані дози брекспіпразолу 1 або 2 мг/добу, демонструючи статистично значущу ефективність препарату в дозі 2 мг/добу порівняно з плацебо. Дані другого дослідження з гнучкою схемою дозування (0,5–2 мг брекспіпразолу на добу) підтвердили значуще поліпшення стану пацієнтів порівняно з учасниками групи приймання плацебо. А в третьому використовували фіксовані дози 2 або 3 мг/добу, і в загальній групі терапії брекспіпразолом спостерігали статистично значуще поліпшення порівняно з групою використання плацебо. Учасники всіх трьох дослідженнях добре переносили брекспіпразол.
Метою дослідження Y. Nakamura etal. (за участю пацієнтів азіатського походження) було підтвердити ефективність і хорошу переносимість брекспіпразолу для лікування пацієнтів з ажитацією за деменції, спричиненої ХА, а також визначити оптимальну дозу згаданого препарату. Брекспіпразол у дозі 2 мг/добу використовували на основі результатів раніше проведених міжнародних досліджень, а дозу 1 мг/добу — для встановлення залежності доза-відповідь.
Матеріали та методи дослідження
вгоруПацієнти
Критерії включення:
- Вік пацієнтів 55–90 років; діагноз деменції альцгеймерівського типу відповідно до Діагностичного та статистичного посібника з психічних розладів п’ятого видання (DSM-5) (APA, 2013).
- Діагноз ХА, встановлений згідно з критеріями Національного інституту неврологічних і комунікативних розладів та інсульту та Асоціацією з вивчення ХА і пов’язаних із нею розладів (NINCDS-ADRDA) (McKhann etal., 1984).
- Наявність опікуна, який міг би надавати інформацію про пацієнта, необхідну для оцінювання стану хворого; загальний показник 1–22 бали під час скринінгового тесту за Короткою шкалою оцінювання психічного статусу (MMSE) (Folstein etal., 1975).
- Показник ≥ 4 бали за доменом ажитації / агресії (частота × тяжкість) нейропсихіатричного опитувальника для комплексного оцінювання психопатологічних порушень за деменції (NPI) (Cummings etal., 1994). Зокрема під час скринінгового тесту та базового оцінювання стану за його версією для геріатричних будинків (NPI-NH) (Wood etal., 2000).
- Постійні або часті рецидиви ажитації, що позначаються на повсякденній активності упродовж ≥ 2 тижнів як до скринінгового тесту, так і до базового оцінювання стану (визначення ажитації відповідало консенсусному визначенню Міжнародної психогеріатричної асоціації) (Sano etal., 2024).
- Щонайменше три випадки агресії з вербальними або фізичними проявами протягом двох тижнів до базового оцінювання.
Критерії виключення:
- Деменція іншого, ніж альцгеймерівський, типу.
- Порушення пам’яті.
- Діагностовані делірій, розлади спектра шизофренії та інші психотичні розлади.
- Біполярний афективний розлад.
- Великий депресивний розлад (ВДР) відповідно до критеріїв DSM-5.
- Попередня терапія антипсихотичними препаратами.
- Стан, резистентний до лікування.
Дизайн
Багатоцентрове рандомізоване подвійне сліпе контрольоване плацебо порівняльне дослідження фази 2/3 із паралельними групами охоплювало період скринінгу тривалістю до 42 днів, період лікування тривалістю 10 тижнів і період подальшого спостереження тривалістю 28 днів. Учасників дослідження рандомізували у співвідношенні 3: 4: 4 для отримання брекспіпразолу в дозі 1 або 2 мг/добу, або плацебо протягом 10 тижнів.
Терапію брекспіпразолом розпочинали з дози 0,5 мг на першому тижні, далі дозу збільшували до 1 мг на другому тижні (8-й день) і надалі — до 2 мг на третьому тижні (15-й день) для групи приймання препарату в дозі 2 мг/добу. Схему титрування та тривалість періоду лікування було визначено на підставі даних попередніх досліджень (Grossberg etal., 2020; Lee etal., 2023).
Брекспіпразол або плацебо приймали перорально раз на добу. Одночасне застосування препаратів антидементних препаратів, наркотичних аналгетиків, β-адреноблокаторів і снодійних було дозволено з обмеженнями.
Оцінювання результатів
вгоруПервинний кінцевий результат
Зміна загального показника за CMAI від базового рівня до 10-го тижня була первинною кінцевою точкою (Cohen-Mansfield, 1989, 1991; Finkel etal., 1992). Цей показник розраховували як суму балів за 29 пунктами визначення ажитованої поведінки, причому кожен пункт оцінювали від 1 (ніколи) до 7 балів (кілька разів на годину), тобто загальний діапазон становив від 29 до 203 балів.
Вторинні кінцеві результати
Вторинними результатами були зміни показників за підшкалами CMAI (зокрема, для оцінювання агресивної / неагресивної поведінки з фізичними проявами та ажитованої поведінки з вербальними ознаками) від вихідного рівня до 10-го тижня втручання; зміна показників за шкалами оцінювання загального клінічного враження — тяжкості захворювання (CGI-S) та загального поліпшення (CGI-I) від вихідного рівня до 10-го тижня (Guy, 1976).
Інші результати
Показники за MMSE і за шкалою оцінювання повсякденної активності згідно з Кооперативним дослідженням ХА (ADCS-ADL) вважали іншими кінцевими результатами (Galasko etal., 1997).
Безпека лікування
Кінцевими результатами щодо безпеки під час лікування були дані про побічні явища, фізикальне обстеження, результати лабораторних тестів, життєво важливі показники, масу тіла пацієнтів, показники 12-канальної електрокардіографії, за шкалами оцінювання екстрапірамідних симптомів, індукованих лікарськими засобами (DIEPSS) та аномальних мимовільних рухів (AIMS) (Inada etal., 2003; Guy, 1976); шкалою оцінювання акатизії Барнса (BARS) (Barnes, 1989); шкалою відстеження ознак суїцидальності Шихана (S-STS) (Coric etal., 2009).
Статистичний аналіз
Розрахунок розміру вибірки ґрунтувався на припущенні різниці для застосування брекспіпразолу 2 мг і плацебо -5,35 (стандартне відхилення [SD] = 15,06) щодо зміни загального бала CMAI від вихідного рівня до 10-го тижня втручання. Згідно з проведеними розрахунками, розміри вибірок (111, 148 і 148 пацієнтів у групах використання терапії брекспіпразолом у дозах 1 або 2 мг/добу або приймання плацебо відповідно) мали забезпечити статистичну потужність дослідження ≥ 86,1 % для брекспіпразолу в дозі 2 мг/добу порівняно з плацебо та ≥ 80,5 % для брекспіпразолу в дозі 1 мг/добу порівняно з плацебо за коефіцієнта α = 0,05.
Аналізована вибірка охоплювала пацієнтів, яких рандомізували для отримання принаймні однієї дози досліджуваного препарату або плацебо, оцінюючи загальний показник за CMAI на початковому рівні та щонайменше один раз після цього.
Як зазначають дослідники, аналіз первинного результату здійснювали за допомогою змішаних моделей для повторних вимірювань (MMRM) для розрахунку відповідних середніх значень за методом найменших квадратів (LS) для кожної групи, а також різниці середніх LS та їхніх двобічних 95 % довірчих інтервалів (ДІ) для груп терапії брекспіпразолом порівняно з плацебо. Вторинні результати аналізували в подібний спосіб. Безпеку лікування визначали за даними всієї аналізованої вибірки пацієнтів. Усі підрахунки виконували за допомогою програмного забезпечення SAS версії 9.4 (SAS Institute, Cary, NC, USA).
Результати дослідження
вгоруПацієнти
Дослідження тривало з 20 серпня 2018 року до 15 травня 2023 року; 410 пацієнтів, які відповідали критеріям включення, рандомізували до трьох груп: 112 і 149 осіб отримували брекспіпразол у дозах 1 або 2 мг/добу відповідно, а 149 — плацебо (далі групи лікування описано в такому порядку).
Показники завершення дослідження становили 74,1 % (83/112); 68,5 % (102/149) і 77,9 % (116/149) відповідно. У всіх групах найчастішою причиною припинення дослідження були побічні явища: у 12,5 % (14/112); 25,5 % (38/149) і 16,8 % (25/149) відповідно.
Отримані дані щодо всіх рандомізованих пацієнтів використовували для оцінювання рівня безпеки; ефективності втручань на основі даних 108, 148 і 147 учасників у кожній групі відповідно. Вихідні демографічні та клінічні характеристики були подібними в усіх групах дослідження. Середні загальні показники за CMAI становили 62,1; 64,1 і 62,7 бала відповідно, а середні показники за CGI-S — 4,5; 4,6 і 4,6 бала відповідно.
Первинний кінцевий результат
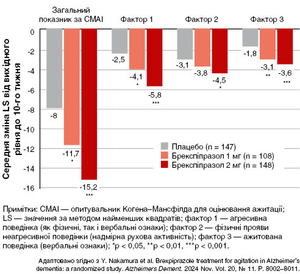
Середні зміни загальних показників за CMAI від базового рівня до 10-го тижня, визначені за методом найменших квадратів (± стандартна похибка) у групах терапії брекспіпразолом у дозах 1 і 2 мг/добу і приймання плацебо становили: -11,7 (± 1,20); -15,2 (± 1,05) і -8,0 (± 1,03) бала відповідно.
Для обох груп лікування брекспіпразолом було продемонстровано статистично значуще поліпшення порівняно з групою плацебо: за дози 2 мг/добу середня різниця становила -7,2 (95 % ДІ від -10,0 до -4,3); p < 0,0001; за дози 1 мг/добу -3,7 (95 % ДІ від -6,8 до -0,7); p = 0,0175. Різниця порівняно з плацебо була більшою для терапії брекспіпразолом у дозі 2 мг/добу (рис. 1).

В обох групах лікування брекспіпразолом, спостерігалося зменшення середніх загальних показників за CMAI: за дози 2 мг/добу — із 4-го тижня (p < 0,01) і продовжувалося на 6-му (p < 0,001), 8-му (p < 0,0001) і 10-му тижнях (p < 0,001); за дози 1 мг/добу — на 8-му і тривало до 10-го тижня (p < 0,05) (рис. 1).
Вторинні кінцеві результати
Під час оцінювання змін показників за підшкалами CMAI від вихідного рівня до 10-го тижня було отримано подібні результати. Зокрема, спостерігалося поліпшення показників за всіма підшкалами (оцінювання агресивної / неагресивної поведінки з фізичними проявами та ажитованої поведінки з вербальними ознаками) у групах терапії брекспіпразолом (1 і 2 мг/добу) порівняно з групою приймання плацебо (p < 0,05 для кожної), за винятком показника щодо неагресивної поведінки з фізичними симптомами в групі терапії брекспіпразолом у дозі 1 мг/добу (поліпшення було статистично незначущим; p > 0,05).
Різниця щодо ефективності лікування порівняно з плацебо була більшою для групи терапії брекспіпразолом у дозуванні 2 мг/добу (рис. 2).
Для інших вторинних кінцевих точок ефективності втручань — зміна показників за шкалами CGI-S і CGI-I від початкового рівня до 10-го тижня — отримано подібні результати: поліпшення в групах терапії брекспіпразолом у дозах 1 і 2 мг/добу порівняно з групою приймання плацебо (p < 0,01 і p < 0,0001 відповідно); різниця порівняно з прийманням плацебо була більшою для групи застосування брекспіпразолу в дозі 2 мг/добу.
Інші результати
Середні зміни інших показників за методом найменших квадратів (± стандартна похибка) від вихідного рівня до останнього візиту були незначними. Зокрема, для груп лікування брекспіпразолом у дозах 1 і 2 мг/добу і приймання плацебо зміни показників за ADCS-ADL становили: -0,6 (± 0,52) бала; -0,8 (± 0,46) бала і 0,7 (± 0,44) бала відповідно; зміни показників за MMSE — -0,7 (± 0,34) бала; -0,3 (± 0,30) і 0,0 (± 0,29) відповідно. Клінічно значущих змін не виявлено.
Результати щодо безпеки
Частота побічних ефектів у групах терапії брекспіпразолом (1 і 2 мг/добу) і приймання плацебо становила 76,8 % (86/112); 84,6 % (126/149) і 73,8 % (110/149) відповідно. У групі лікування брекспіпразолом у дозі 1 мг/добу трапилося два випадки побічних явищ із смертельним наслідком, тоді як за дози 2 мг/добу і приймання плацебо летальних випадків не спостерігалося.
Загальна частота летальних випадків серед пацієнтів, які приймали брекспіпразол, становила 0,8 % (2/261). Частота серйозних побічних реакцій у групах терапії брекспіпразолом у дозуваннях 1 і 2 мг/добу і приймання плацебо становила: 6,3 % (7/112); 6,0 % (9/149) і 4,7 % (7/149) відповідно; частота тяжких небажаних ефектів: 7,1 % (8/112); 10,1 % (15/149) і 6,7 % (10/149) відповідно; частота побічних ефектів, які призвели до припинення приймання досліджуваного препарату: 12,5 % (14/112); 25,5 % (38/149) і 16,8 % (25/149) відповідно.
Із частотою ≥ 5 % у загальній групі терапії брекспіпразолом спостерігалися такі побічні ефекти, як сонливість, брадикінезія, безсоння, гіперсалівація, ригідність м’язів, порушення ходи, падіння, лихоманка; ускладнення, пов’язані із седацією; контузія та зниження апетиту.
Тяжкість більшості TEAE була легкою або помірною. У двох летальних випадках причинами смерті учасників дослідження стали серцеві захворювання та аспіраційна пневмонія. Як зазначають Y. Nakamura etal., вони не були пов’язані з прийманням брекспіпразолу. Єдиним серйозним побічним явищем, що виникло у двох або більше пацієнтів будь-якої групи терапії брекспіпразолом, була аспіраційна пневмонія (1,8 % [2/112] і 1,3 % [2/149] у групах приймання брекспіпразолу в дозах 1 і 2 мг/добу відповідно); лише один випадок у групі терапії брекспіпразолом (1 мг/добу) дослідники вважали пов’язаним із застосуванням препарату.
Частота побічних ефектів, пов’язаних з екстрапірамідними симптомами у групах терапії брекспіпразолом у дозах 1 і 2 мг/добу і приймання плацебо становила 25,9; 32,2 і 7,4 % відповідно. Середні зміни загальних показників за DIEPSS (± стандартна похибка) від вихідного рівня до останнього візиту становили 1,0 (± 0,22); 1,6 (± 0,19) і 0,0 (± 0,19) бала відповідно. Показники за AIMS та BARS були < 1,0 бала у всіх групах; клінічно значущих змін показників за S-STS не виявлено.
У всіх групах дослідження не спостерігалося клінічно значущих змін і помітних відмінностей щодо даних лабораторних досліджень, життєво важливих показників, маси тіла, індексу маси тіла і показників електрокардіографії в дванадцяти відведеннях.
Частка пацієнтів із визначеним клінічно значущим збільшенням маси тіла на ≥ 7 % у групах терапії брекспіпразолом у дозах 1 і 2 мг/добу і приймання плацебо становила: 2,9 % (3/104); 6,2 % (9/145) і 2,8 % (4/145), а зниження — 4,8 % (5/104); 4,1 % (6/145) і 2,8 % (4/145) випадків відповідно.
Обговорення
вгоруЗа первинним кінцевим результатом ефективності (зміна загального показника за CMAI від вихідного рівня до 10-го тижня) терапія брекспіпразолом в обох дозах (1 і 2 мг/добу) сприяла статистично значущому поліпшенню стану порівняно з плацебо, ефект лікування був більшим за вищої дози препарату.
Щодо вторинних результатів ефективності (зміни показників за підшкалами CMAI, зміни показників за CGI-S від початкового рівня до 10-го тижня, і показників за CGI-I на 10-му тижні), спостерігали подібні результати, за винятком того, що поліпшення балів за субшкалою CMAI 2 (фізичні ознаки неагресивної поведінки) у групі застосування брекспіпразолу (1 мг) було статистично незначущим.
Поліпшення показників відбувалося не лише за субшкалами агресивної та ажитованої поведінки з вербальними проявами, але й за субшкалою неагресивної поведінки з фізичними ознаками. Зокрема, поліпшення середніх змін загального показника за CMAI раніше фіксували в разі застосування брекспіпразолу в дозуванні 2 мг/добу (із 4-го тижня; p < 0,01), ніж у дозі 1 мг/добу (із 8-го тижня; p < 0,05).
Лікування брекспіпразолом в обох дозах є ефективним і в разі збільшення дозування препарату можна очікувати на раніше бажаний результат. Частота побічних ефектів була вищою в групі терапії брекспіпразолом у дозі 2 мг (84,6 %), ніж у дозі 1 мг (76,8 %), і в групі приймання плацебо (73,8 %), а частота таких наслідків, що призводили до припинення досліджуваного лікування, була більшою для групи терапії в дозі 2 мг/добу (25,5 %), ніж у дозі 1 мг/добу (12,5 %) і групі приймання плацебо (16,8 %). Більшість побічних реакцій мали легкий або середній ступінь тяжкості, обидві дози брекспіпразолу учасники дослідження переносили добре.
У подібному попередньому дослідженні за участю пацієнтів із деменцією, спричиненою ХА, і ознаками ажитації, для загальної групи терапії брекспіпразолом (у фіксованих дозах 2 або 3 мг/добу) було продемонстровано статистично значуще поліпшення порівняно з групою приймання плацебо щодо первинного кінцевого результату ефективності (зміна загального показника за CMAI від вихідного рівня до 12-го тижня).
Частота побічних ефектів у загальній групі застосування брекспіпразолу та плацебо становила 40,7 і 31,0 % відповідно, а частота небажаних явищ, що призводили до припинення досліджуваного лікування, — 5,3 і 4,3 % відповідно (Lee etal., 2023).
Примітно, що в попередньому дослідженні ≥ 90 % пацієнтів були представниками білої раси, їхній середній вік становив 73–75 років, а середня маса тіла — 70–71 кг, тоді як у дослідженні Y. Nakamura etal. усі пацієнти були азіатами, мали вищий середній вік (~ 80 років) та нижчу середню масу тіла (~ 48 кг).
Вища частота побічних ефектів як у групах терапії брекспіпразолом, так і в групі приймання плацебо в другому дослідженні, на думку авторів, може бути пов’язана з відмінностями саме в цих характеристиках пацієнтів.
У попередньому дослідженні з використанням фіксованих доз брекспіпразолу (1 або 2 мг/добу) статистично значуще поліпшення зміни загального показника за CMAI від вихідного рівня до 12-го тижня виявлено лише для групи осіб, які приймали вищу дозу препарату (Grossberg etal., 2020).
Тоді як у дослідженні Y. Nakamura etal. було продемонстровано статистично значуще поліпшення цього показника в обох групах терапії брекспіпразолом (у дозах 1 і 2 мг/добу). Щодо безпеки застосування атипових антипсихотичних препаратів, то для цієї популяції пацієнтів досліджували ризик смерті, екстрапірамідних симптомів, збільшення ваги та розвитку метаболічного синдрому (Burghardt etal., 2018; Yunusa etal., 2019).
Дві смерті, зафіксовані під час дослідження Y. Nakamura etal., дослідники вважали не пов’язаними з терапією брекспіпразолом; не виявлено також клінічно значущих змін суїцидальності, оціненої за S-STS.
Терапія брекспіпразолом асоціювалася з вищою частотою екстрапірамідних симптомів, ніж приймання плацебо. Однак, за показниками за шкалами DIEPSS, AIMS і BARS, вплив препарату був незначущим або взагалі не спостерігався. Не виявлено також значущих змін маси тіла та індексу маси тіла.
Побічні ефекти, пов’язані з порушенням мозкового кровообігу, сонливість / седація, падіння / переломи / травми та нетримання сечі / інфекції сечовивідних шляхів є відомими побічними ефектами за терапії атиповими антипсихотичними засобами (Yunusa etal., 2019).
Зокрема, у дослідженні Y. Nakamura etal. сонливість та ускладнення, пов’язані із седацією, спостерігали із частотою ≥ 5 % і в ≥ 2 рази частіше в обох групах застосування брекспіпразолу (1 і 2 мг/добу), ніж плацебо: сонливість із частотою 8,0; 16,1 і 2,0 %; ускладнення, пов’язані із седацією — 2,7; 7,4 і 1,3 % відповідно. Проте частота інших побічних ефектів не була вищою за використання брекспіпразолу, ніж плацебо.
Ризик смерті впродовж проведення дослідження, як зазначають автори, не збільшувався; така тенденція також спостерігалася в межах проведеного масштабного проспективного когортного випробування H. Arai etal. (2016). У цьому дослідженні частка учасників, які були пацієнтами лікувальних або геріатричних закладів, становила близько 30 %.
Висновки
вгоруРезультати представленого дослідження підтвердили, що лікування брекспіпразолом (1 і 2 мг/добу) протягом 10 тижнів сприяє статистично значущому поліпшенню загального показника за CMAI порівняно з прийманням плацебо. На тлі терапії брекспіпразолом було зафіксовано поліпшення вторинних кінцевих результатів. Загалом лікування вказаним препаратом в обох дозах добре переносилося. Схема лікування брекспіпразолом у початковій дозі 0,5 мг/добу з подальшим її збільшенням до 1 або 2 мг/добу дає змогу ефективно і безпечно зменшити виразність ознак ажитації у пацієнтів із деменцією, спричиненою ХА.
Як зазначають Y. Nakamura etal., можливість контролювати тяжкість і частоту ажитації за допомогою брекспіпразолу в амбулаторних умовах запобігає ранній госпіталізації таких пацієнтів.
Підготувала Наталія Купко
Наш журнал
в соцсетях:
Мнения экспертов
Выпуски за 2025 Год
Содержание выпуска 10 (165), 2025
Содержание выпуска 9 (164), 2025
Содержание выпуска 8 (163), 2025
-
Всесвітній день психічного здоров’я: належна підтримка пацієнтів як суспільний пріоритет
-
Посттравматичний стресовий розлад, спричинений війною: аналіз на основі літературних образів
-
Нейрогенний синдром грудного виходу: пошук оптимального підходу до лікування
-
Минуле та сьогодення Української протиепілептичної ліги: тридцять років складного та успішного шляху
-
Падіння в похилому віці: оцінювання ризику, аспекти профілактики й менеджменту
-
Тернистий шлях застосування бензодіазепінів: від величі до забуття та можливого відродження
-
Досягнення та підтримання стану ремісії в пацієнтів із великим депресивним розладом
Содержание выпуска 7 (162), 2025
-
Минуле та сьогодення Української протиепілептичної ліги: тридцять років складного та успішного шляху
-
Можливості фармакотерапії за уражень мозку, що супроводжуються порушенням свідомості
-
Застосування високих доз оланзапіну в лікуванні пацієнтів із резистентними формами шизофренії
-
Лікування пацієнтів із нейропатичним болем на первинній ланці допомоги
Содержание выпуска 6 (161), 2025
-
Вплив соціальних мереж на психічне здоров’я дітей і підлітків
-
П’ять порад батькам, як знизити вплив соціальних мереж на дитину / підлітка
-
Минуле та сьогодення Української протиепілептичної ліги: тридцять років складного та успішного шляху
-
Діагностична цінність клінічного оцінювання когнітивних функцій
-
Вплив війни на психічне здоров’я молоді: роль резилієнсу та психологічних інтервенцій
-
Фармакотерапія пацієнтів із деменцією: первинна ланка медичної допомоги
-
Методичні рекомендації щодо профілактики професійного вигоряння медичних працівників
Содержание выпуска 5 (160), 2025
-
Поліпшення психологічного стану населення в умовах довготривалої війни
-
Ефективність поетапної програми психологічних втручань для мігрантів
-
Альтернативний підхід до терапії тривожних розладів: важливість правильного титрування дози
-
Аналіз ефективності фармакотерапії депресії у жінок дітородного віку
-
Модель поетапного лікування пацієнтів із ноцицептивним болем
Содержание выпуска 4 (159), 2025
-
Психіатрія способу життя: нові горизонти для психічного здоров’я
-
Поліпшення функціонування як ключова мета лікування пацієнтів із великим депресивним розладом
-
Розлади харчової поведінки: серйозність проблеми та сучасні підходи до її вирішення
-
Антидепресант із мультимодальною дією: можливості застосування міансерину в клінічній практиці
-
Сучасні підходи до діагностування та лікування пацієнтів із кататонією
-
Фармакологічне лікування пацієнтів із шизофренією та пов’язаними з нею психозами
Содержание выпуска 3 (158), 2025
-
Всесвітній день поширення інформації про аутизм: спростовуємо поширені міфи
-
Резистентна до лікування депресія: можливості аугментації терапії
-
Фармакотерапія тривожних розладів і нейропротекція: альтернатива бензодіазепінам
-
Лікування пацієнтів підліткового віку із шизофренією: ефективність і безпека антипсихотичної терапії
-
Лікування депресії в пацієнтів з ішемічною хворобою серця або ризиком її розвитку
-
Профілактична фармакотерапія епізодичного мігренозного головного болю в амбулаторних умовах
-
Стратегії зниження дозування бензодіазепінів: коли ризики переважають користь
Содержание выпуска 1, 2025
-
Когнітивні порушення судинного генезу: діагностування, профілактика та лікування
-
Лікування ажитації за деменції, спричиненої хворобою Альцгеймера
-
Постінсультні нейропсихіатричні ускладнення: типи, патогенез і терапевтичні втручання
-
Перспективи застосування препаратів на основі рослинних компонентів для лікування депресії
-
Застосування диклофенаку за неврологічних станів: перевірена ефективність і пошук нових підходів
-
Постінсультний емоціоналізм: патофізіологія, поширеність та лікування
Содержание выпуска 2 (157), 2025
-
Деякі питання запровадження оцінювання повсякденного функціонування особи
-
Важливість співвідношення «доза-ефект» при застосуванні нестероїдних протизапальних препаратів
-
Медикаментозний паркінсонізм: причини, наслідки та шляхи уникнення
-
Фармакотерапія пацієнтів із шизофренією: важливість поліпшення рівня соціальної залученості
Содержание выпуска 1 (156), 2025
-
Підтримка психічного здоров’я на первинній ланці надання медичної допомоги
-
Лікування депресії в літніх пацієнтів: вплив на патофізіологію розладу, ефективність та безпека
-
Нестероїдні протизапальні препарати: багаторічний досвід та особливості застосування
-
Фармакотерапія великого депресивного розладу: пошук антидепресантів з оптимальною ефективністю
Выпуски текущего года
Содержание выпуска 4 (169), 2026
-
Індивідуалізована антипсихотична терапія з урахуванням тютюнокуріння
-
Консенсус щодо виявлення й ведення пацієнтів із депресією та коморбідним больовим синдромом
-
Сучасні підходи до застосування кеторолаку при гострому болю в неврологічній практиці
-
Ведення пацієнтів із хворобою Паркінсона: огляд ключових рекомендацій
Содержание выпуска 3 (168), 2026
-
Розширення ролі носимих медичних пристроїв у сучасній неврологічній практиці
-
Роль мистецтва в реабілітації та поліпшенні ментального здоров’я
-
Венлафаксин у терапії ПТСР: від доказової бази до вибору індивідуальної стратегії
-
Нові підходи, сміливі ідеї та найактуальніші теми у сфері неврології
-
Міастенія під маскою депресії та тривоги: клінічні пастки для психіатра і тактика ведення пацієнта
-
Нейропротекція та когнітивна реабілітація в сучасній психіатрії: фокус на комбіновану терапію
-
Антидепресант тразодон: фармакологічний профіль та мультимодальні й мультифункціональні ефекти
-
Рекомендації щодо ведення пацієнтів із нейропатичним болем унаслідок травми спинного мозку
Содержание выпуска 1, 2026
-
Штучний інтелект у геріатричній психіатрії: поєднання точності з людським досвідом
-
Синдром старечої астенії та деменція: клінічні виклики і сучасні рекомендації
-
Реабілітація, відновлення та повернення пацієнтів до активного життя після інсульту
-
Порушення когнітивних функцій, деменція та депресія у літніх осіб
Содержание выпуска 2 (167), 2026
-
Нові підходи, сміливі ідеї та найактуальніші теми у сфері неврології: дебати
-
Нейробореліоз: коли інфекція маскується під неврологічне захворювання
-
Хвороба Вільсона: від неспецифічних скарг до встановлення діагнозу
-
Призначення антипсихотичних препаратів для лікування психічних розладів
-
Підходи до лікування посттравматичного стресового розладу у військових
-
Аспекти реабілітації після інсульту для оптимального функціонального відновлення пацієнтів
Содержание выпуска 1 (166), 2026
-
Психіатрична допомога в Україні у 2025 році: що реально змінилося для лікаря і пацієнта
-
Дулоксетин: лікування депресивних і тривожних розладів та хронічного болю
-
Нові підходи, сміливі ідеї та найактуальніші теми у сфері неврології
-
Нейробіологічні чинники формування терапевтичної дії плацебо та ноцебо у клінічній практиці
Рассылка
Будьте в курсе последних обновлений – подпишитесь на рассылку материалов на Ваш e-mail
Подписаться








/thumbs/widget_nn25_10-165_titul.jpg)
/thumbs/widget_nn25_9-164_titul.jpg)
/thumbs/widget_nn25_8-163_titul_.jpg)
/thumbs/widget_nn25_7-162_titul-1.jpg)
/thumbs/widget_nn25_6-161_titul.jpg)
/thumbs/widget_nn25_5-160_titul.jpg)
/thumbs/widget_nn25_4-159_titul-1.jpg)
/thumbs/widget_nn25_3-158_titul.jpg)

/thumbs/widget_nn25_2-157_titul-1.jpg)
/thumbs/widget_nn25_1-156_titul-1.jpg)
/thumbs/widget_nn26_4-169_titul.jpg)
/thumbs/widget_nn26_3-168_titul.jpg)

/thumbs/widget_nn26_2-167_titul.jpg)
/thumbs/widget_nn26_1-166_titul.jpg)















