Рассылка
Будьте в курсе последних обновлений – подпишитесь на рассылку материалов на Ваш e-mail
Подписаться-
Штучний інтелект у геріатричній психіатрії: поєднання точності з людським досвідом
-
Синдром старечої астенії та деменція: клінічні виклики і сучасні рекомендації
-
Реабілітація, відновлення та повернення пацієнтів до активного життя після інсульту
-
Порушення когнітивних функцій, деменція та депресія у літніх осіб
Порушення когнітивних функцій, деменція та депресія у літніх осіб
Зміст статті:
- Аналіз літератури й термінологія
- Спільні й відмінні когнітивні порушення при депресії та деменції
- Депресія як чинник ризику розвитку деменції
- Депресія як продромальний симптом деменції
- Депресія як розлад особистості, пов’язаний із ППСД
- Сумісна дія антидепресантів і засобів протидементної терапії на когнітивні функції та настрій
- Висновки
Порушення когнітивних функцій і депресія є одними з найпоширеніших нейропсихіатричних станів у літніх осіб і часто мають спільні нейробіологічні механізми. В огляді Y. J. Jang et al. «Cognitive impairment, dementia and depression in older adults» (J Clin Med, 2026; 15 (3): 1198) узагальнено сучасні дані про подібність і відмінність когнітивних профілів депресії та деменції, роль депресії як продромального або коморбідного прояву деменції та двоспрямовані ефекти лікування. Пропонуємо до вашої уваги основні положення цієї публікації.
Депресія в літньому віці асоційована з підвищеним ризиком легких порушень когнітивних функцій (ПКФ) і деменції таможе посилювати їх перебіг; водночас когнітивні порушення часто спричиняють розвиток депресії. Дляобох станів характерні дефіцит уваги, порушення виконавчих функцій і швидкості обробки інформації (ШОІ). Поняття «псевдодеменція» нині переглянуто: симптоми депресії можуть бути раннім проявом нейродегенерації (Ren et al., 2024).
Серед спільних патофізіологічних механізмів депресії та деменції — цереброваскулярні порушення, дисрегуляція гіпоталамо-гіпофізарно-наднирникової осі, нейрозапалення і зниження нейропластичності. Пізня депресія пов’язана зі змінами лобово-стріатумної/лімбічної систем і гіперінтенсивністю білої речовини (ГБР), що лежить в основі концепції «судинної депресії» (Taylor etal., 2013). За деменції депресія часто входить до складу поведінкових та психологічних симптомів (ППСД) (Kales etal., 2019).
Терапевтично важливо враховувати взаємовплив настрою та когнітивних функцій (КФ). Під час лікування антидепресанти (АД) можуть поліпшувати окремі когнітивні домени у літніх осіб без деменції, тоді як ноотропи спрямовані на корекцію поведінкових симптомів (Pozuelo Moyano et al., 2025).
Y. J. Jang etal. (2026) пропонують інтегровану модель, що виділяє депресію як фактор ризику, продромальний прояв або компонент ППСД на різних стадіях захворювання, а також зіставити клінічні фенотипи з їхньою біологічною основою та наслідками лікування.
Аналіз літератури й термінологія
вгоруПошук у базах даних PubMed та Google Scholar охопив публікації з січня 2000 р. по березень 2025 р. Перевагу надавали метааналізам і когортним, нейровізуалізаційним, біомаркерним та масштабним рандомізованим контрольованим дослідженням (РКД) за участю осіб літнього віку.
За результатами аналізу виокремлено такі ключові терміни та дефініції:
- Депресія пізнього віку — депресивні синдроми в осіб віком ≥ 60 років, незалежно від віку дебюту.
- Депресія з пізнім початком — дебют у віці 60–65 років, часто пов’язаний із цереброваскулярною та нейродегенеративною патологіями.
- Продромальна депресія — симптоми депресії в часовій близькості до дебюту деменції за наявності біологічних ознак нейродегенеративних або судинних змін.
- Виконавча дисфункція — порушення процесів контролю (переключення уваги, гальмування, робоча пам’ять), пов’язані з ураженням лобово-підкіркових ланцюгів.
- Суб’єктивне ПКФ (СПКФ) — самостійно оцінене погіршення КФ за відсутності об’єктивно підтверджених порушень.
Спільні й відмінні когнітивні порушення при депресії та деменції
вгоруПКФ за депресії та деменції пізнього віку часто включають погіршення уваги, ВФ і ШОІ, що зумовлює значне перекриття нейропсихологічних профілів. За великого депресивного розладу в літніх осіб типові порушення ШОІ та ВФ пов’язані з дисфункцію лобово-підкіркових ланцюгів; подібні зміни на ранніх стадіях деменції можуть передувати розладам пам’яті (Liampas etal., 2024). Це ускладнює диференціацію оборотної «псевдодеменції» та ранньої нейродегенерації.
Диференціальну діагностику в клінічній практиці ускладнює те, що ступінь та характер ПКФ при депресії пізнього віку неоднорідні й варіюють залежно від таких чинників, як:
- підтип депресії;
- тяжкість симптомів;
- тип лікування;
- когнітивний резерв.
Між когнітивними профілями депресії та деменції є важливі відмінності. При хворобі Альцгеймера (ХА) переважає дефіцит кодування й зберігання нової інформації, тоді як при депресії — порушення відтворення за відносно збереженого розпізнавання. Когнітивний дефіцит при депресії частково оборотний на тлі ефективної терапії, тоді як для деменції характерне прогресування й переважна незворотність ПКФ (Pozzoli et al., 2018).
Нейровізуалізаційно обидва стани пов’язані з порушеннями фронтолімбічних мереж, однак при депресії зміни здебільшого мають судинно-функціональний характер (гіперінтенсивність білої речовини, порушення перфузії), тоді як при деменції — дегенеративно-структурний (атрофія гіпокампа, накопичення β-амілоїду й τ-протеїну) (Chen et al., 2021).
Розпізнавання континууму «від депресії через когнітивні порушення до деменції» важливе для клінічної практики. Літні особи із пізнім початком депресії, виразною виконавчою дисфункцією та високим тягарем ГБР мають підвищений ризик подальшого ПКФ та переходу в деменцію (Masse etal., 2021). Оцінювання їхнього нейропсихологічного стану має включати не тільки виявлення розладів настрою, але й тривалий моніторинг КФ, особливо доменів ШОІ та контролю ВФ, застосування нейровізуалізації або оцінювання біомаркерів, якщо ПКФ зберігається, попри поліпшення настрою, або супроводжується виразною виконавчою дисфункцією чи наявністю значної кількості вогнищ ГБР (Brailean etal., 2017). Розуміння спільних і відмінних рис ПКФ за депресії та деменції дозволяє точніше стратифікувати ризик й обирати належні стратегії втручання.
Депресія як чинник ризику розвитку деменції
вгоруМетааналізи свідчать, що депресія є незалежним фактором ризику деменції з тривалим латентним періодом і відсутністю біологічних маркерів неминучих нейродегенеративних змін. Комплексний метааналіз даних 23 когортних досліджень показав, що депресія в пізньому віці пов’язана із підвищеним (на 85 %) ризиком деменції з усіх причин, а при оцінюванні підтипів мала місце сильніша кореляція для судинної деменції, ніж для ХА (Diniz etal., 2013). Інші популяційні дослідження й систематичні огляди підтвердили асоціацію депресивних розладів із вищою частотою розвитку ЛПКФ та деменції (Ownby etal., 2006; Byers, Yaffe, 2011). У масштабному випробуванні було показано цей зв’язок для депресії раннього, середнього та пізнього віку після корекції з урахуванням освіти, рівня доходу, наявності серцево-судинних патологій, цукрового діабету та супутніх психічних захворювань (Elser etal., 2023). Когортне дослідження за участю осіб після 75 років показало, що вплив депресії на ризик деменції, ймовірно, послаблюється з віком (Jang etal., 2025). Масштабне поздовжнє випробування продемонструвало поступове зростання ризику деменції зі збільшенням кумулятивного тягаря симптомів депресії та поганої відповіді на лікування. Це підтвердило, що тяжкість депресії є клінічно значущим стратифікаційним фактором ризику (Chu etal., 2025).
Запропоновано кілька біологічних механізмів зв’язку між депресією та пізнішою деменцією, в яких судинна патологія відіграє особливо важливу роль. Дані нейровізуалізаційних і нейропатологічних досліджень свідчать, що в осіб літнього віку із депресією часто спостерігаються підвищений рівень мозкового кровотоку, лакунарні інфаркти та захворювання дрібних судин, що призводить до так званої судинної депресії. Ці цереброваскулярні зміни можуть порушувати лобово-підкіркові й лімбічні ланцюги, які є важливими для регуляції ВФ та емоцій, забезпечуючи вірогідний механістичний місток між порушенням настрою і ПКФ (Alexopoulos, 2019).
Судинна патологія може бути як спільним етіологічним фактором депресії та ПКФ, так і медіатором, через який депресія прискорює нейродегенеративні зміни. І навпаки, хоча патологічні механізми ХА — накопичення β-амілоїду і τ-протеїну — вважаються основою взаємозв’язку депресії та деменції, біологічні докази прямої кореляції залишаються суперечливими. Систематичний огляд та метааналіз даних досліджень ліквору, плазми й результатів позитронно-емісійної томографії не виявив зв’язку між навантаженням β-амілоїдом та депресією у літніх осіб без деменції, але аналіз підгруп (переважно осіб із ЛПКФ або депресією пізнього віку) показав можливу асоціацію із ПКФ (Twait etal., 2024).
Підтверджено роль нейрозапальних і окиснювальних механізмів у континуумі депресії–деменції:
- Підвищені рівні периферичних запальних маркерів, зокрема інтерлейкіну-6, пов’язані з депресією в пізньому віці.
- Активація мікроглії та дисрегуляція гіпоталамо-гіпофізарно-наднирникової осі спричиняють вразливість, зумовлену нейродегенерацією.
- Біомаркери оксидативного стресу, як-от нітротирозин, є предикторами деменції у літніх осіб із депресією.
Отже, хоча депресія може співіснувати з ХА у деяких пацієнтів, сучасні дані свідчать, що не лише накопичення β-амілоїду й τ-протеїну, але й альтернативні біологічні шляхи, що частково перекриваються, можуть призводити до ПКФ.
Депресія як продромальний симптом деменції
вгоруНа відміну від впливу депресії як дистального фактора ризику, концепція депресії як продромального чинника полягає в тому, що її симптоми виникають у безпосередній часовій близькості до початку деменції та супроводжуються клінічними/біологічними ознаками нейродегенеративної/судинної патології. В осіб літнього віку симптоми депресії можуть бути продромальними проявами початкового нейродегенеративного процесу. Так, масштабне когортне дослідження виявило, що в осіб із депресією пізнього віку симптоми деменції значно частіше з’являються в перші роки після встановлення діагнозу (Holmquist etal., 2020). Питання, чи є пізня депресія ранньою стадією ХА або судинної деменції, а не просто коморбідним розладом настрою, є дискусійним (Boparai etal., 2025). Тому важливо розглядати епізоди депресії пізнього віку не лише як предиктори ризику, але й як сигнали розвитку патології мозку.
Дослідження біомаркерів (рівня β-амілоїду в кортикальній мозковій артерії, показника ГБР, порушень лобово-підкіркових ланцюгів) дозволяють виявляти біологічні відмінності продромальних і непродромальних форм депресії пізнього віку. Масштабне дослідження показало, що поєднання депресії пізнього віку та СПКФ пов’язане зі значно вищою частотою виникнення ЛПКФ і деменції порівняно з кожним із цих станів окремо (Yan etal., 2024). Отже, депресивні епізоди, які розвинуться надалі, можуть перетинатися з дуже ранніми нейродегенеративними/судинними змінами в мозку або маскувати їх.
Незважаючи на зростання інтересу до продромальної депресії як раннього прояву деменції, біологічні докази на підтвердження цієї інтерпретації залишаються обмеженими й неоднорідними. Дані нейровізуалізаційних і біомаркерних досліджень про підвищене β-амілоїдне навантаження або судинну патологію при депресії пізнього віку є значною мірою групоспецифічними, перехресними та нерівномірно відтворюваними, а розміри ефекту загалом скромні. Зокрема, метааналізи не продемонстрували послідовного зв’язку β-амілоїдного навантаження та симптомів депресії в осіб літнього віку без когнітивних порушень. Тобто депресію пізнього віку не можна розглядати як характерний біологічний продромальний симптом деменції у більшості пацієнтів. Ці обмеження підкреслюють необхідність обережної інтерпретації даних і проведення поздовжніх біомаркерних досліджень для уточнення часової послідовності та причинно-наслідкового зв’язку.
Розпізнавання депресії як потенційного продромального симптому деменції має важливі прогностичні та клінічні наслідки. У літніх осіб із вперше виявленою депресією, особливо за наявності в них порушень ВФ, СПКФ та нейровізуалізаційних маркерів цереброваскулярних захворювань / уражень гіпокампа, спостерігається швидший розвиток деменції, ніж у пацієнтів без таких ознак (Lyetal., 2021). Тривалий моніторинг КФ є особливо необхідним для осіб похилого віку із вперше виявленою депресією, виконавчою дисфункцією, СПКФ або високим показником ГБР, оскільки ці ознаки можуть свідчити про вищий ризик деменції та потребують застосування нейровізуалізації, оцінювання судинного ризику чи скерування на дослідження біомаркерів. Раннє виявлення переходу від депресивного стану до ПКФ може сприяти своєчасному втручанню й уповільненню прогресування до тяжкої деменції.
Депресія як розлад особистості, пов’язаний із ППСД
вгоруСаме клінічно значущі симптоми депресії, а не підтверджений діагноз великого депресивного розладу є одними із найпоширеніших ППСД. Вони наявні у ~ 30–50 % пацієнтів із ХА і ще більшої частки осіб із деменцією з тільцями Леві (ДТЛ) та лобово-скроневою деменцією (ЛСД). Поширеність клінічно значущої депресії особливо висока при ДТЛ, за якої афективні симптоми часто співіснують із флуктуаціями уваги та зоровими галюцинаціями, а також поведінковому варіанті ЛСД, коли апатія та зміни настрою є чіткими ранніми ознаками (Collins etal., 2023).
Наявність депресії при деменції пов’язана із такими наслідками, як (Botto etal., 2022):
- швидше погіршення когніції та функціонування;
- більший нейропсихіатричний тягар;
- підвищені показники інституціоналізації;
- зниження якості життя пацієнтів і доглядальників.
Низка поздовжніх досліджень також показали вищу смертність і частіші прояви тяжкої ажитації, психозів та втрати самостійності пацієнтів із деменцією та коморбідною депресією, навіть після коригування на початковий рівень тяжкості деменції, судинну коморбідність і тягар нейропсихіатричних симптомів (Fisher etal., 2014). Отже, депресія, що виникає у контексті встановленої деменції, є не просто супутньою патологією, а основним фактором, що визначає перебіг захворювання та результати лікування.
Симптоми депресії при деменції суттєво перетинаються із проявами апатії, але ці синдроми клінічно та прогностично різняться. Для депресії характерні суб’єктивний дистрес, смуток, почуттям провини та негативний афект, апатія ж переважно проявляється порушенням мотивації, емоційного сприйняття й реагування і цілеспрямованої поведінки, часто за відсутності явної дисфорії. При ХА, ДТЛ та ЛСД апатія є поширенішою, ніж епізоди великого депресивного розладу, і сильніше пов’язана із прискореним ПКФ, погіршенням функціонування й збільшенням навантаження на доглядальників (Sep etal., 2022). За наявності апатії ефективність АД обмежена, тоді як інгібітори холінестерази (ІХЕ) й нефармакологічні втручання, спрямовані на залученість та середовищну стимуляцію, єкориснішими (Costello etal., 2023). Нездатність диференціювати депресію від апатії ускладнює відповідь на лікування та прогноз у пацієнтів із деменцією.
За підтвердженої деменції симптоми депресії пов’язані з кількома нейробіологічними механізмами. Нейровізуалізаційні дослідження демонструють структурну атрофію в лімбічних і паралімбічних ділянках, включно із передньою поясною корою, гіпокампом та орбітофронтальною корою, а також порушення мереж пасивного режиму роботи мозку і визначення значущості. Активація нейрозапалення та холінергічний дефіцит запропоновані як допоміжні механізми, особливо при ХА та ДТЛ (dos Santos etal., 2024). Відповідь на лікування також відрізняється від такої в осіб із депресією без деменції. Масштабні РКД показали, що ефективність селективних інгібіторів зворотного захоплення серотоніну (СІЗЗС) при ХА є обмеженою/помірною (He etal., 2021). Натомість продемонстровано помірну користь ІХЕ та мультимодальних нефармакологічних втручань, що включають навчання опікунів та програми структурованої активності (Oba etal., 2022). Це свідчить про необхідність специфічних підходів до лікування депресії як частини ширшого синдрому ППСД.
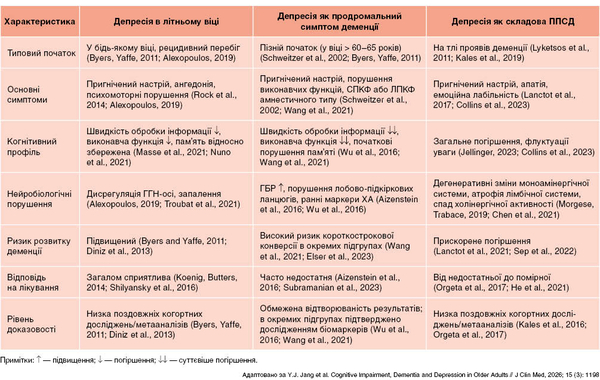
Окрім забезпечення ефективності, фармакотерапія пацієнтів із депресією та ППСД потребує ретельного врахування геріатричної безпеки. Наявні ризики підкреслюють важливість індивідуалізованих рішень щодо лікування, балансу безпеки, контролю симптомів, функціональних результатів та навантаження на доглядальника. Відмінні клінічні й біологічні характеристики депресії пізнього віку, продромальної депресії та депресії на тлі ППСД наведені в таблиці 1.
Сумісна дія антидепресантів і засобів протидементної терапії на когнітивні функції та настрій
вгоруЛікування АД при депресії пізнього віку асоційоване із деякими перевагами щодо поліпшення певних доменів КФ. Кілька клінічних досліджень показали, що СІЗЗС можуть чинити помірний ефект щодо ВФ і ШОІ у літніх осіб без деменції (Koenig etal., 2014; Schulkens etal., 2022). Длязасобів із мультимодальною серотонінергічною дією, як-от вортіоксетин, продемонстровано певну прокогнітивну користь, головним чином щодо ВФ і ШОІ, які, ймовірно, не залежать від поліпшення настрою в осіб похилого віку без деменції (Bishop etal., 2021).
На противагу цьому, результати РКД за участю осіб із ХА суперечливі. Дослідження HTA-SADD та інші масштабні контрольовані випробування не виявили суттєвої переваги СІЗЗС над плацебо щодо зменшення симптомів депресії або поліпшення КФ при ХА. Ймовірно, це відображає обмеження дизайну досліджень: ефект «стелі» (неможливість досягти вищого рівня ефективності) за участю пацієнтів із пізніми стадіями захворювання, діагностична гетерогенність, обмежена чутливість когнітивних кінцевих точок та значна відповідь на плацебо (Orgeta etal., 2017; Costello etal., 2023). Отже, хоча лікування депресії може сприяти помірному поліпшенню КФ в осіб літнього віку без деменції, такі ефекти суттєво зменшуються в контексті прогресування деменції.
І навпаки, фармакотерапія, спрямована на деменцію, чинить помірний вплив на симптоми депресії та апатії, що значною мірою відображає зменшення загального нейропсихіатричного тягаря, а не прямий ефект АД. Терапія ІХЕ (як-от донепезил, ривастигмін та галантамін) сприяє незначному зменшенню проявів депресії, дратівливості та апатії при ХА (Wang etal., 2015). Ці ефекти більш послідовно спостерігаються при ДТЛ, за якої посилення холінергічної передачі може полегшити порушення настрою та поведінки, поліпшити увагу та зменшити флуктуації КФ. Продемонстровано користь застосування ривастигміну при ДТЛ (Madson etal., 2016). Терапія мемантином, антагоністом рецепторів N-метил-D-аспартату, також сприяє зменшенню проявів ажитації та дратівливості, позитивно впливає на симптоми депресії, що радше свідчить про непрямий вплив на настрій, вторинний відносно стабілізації поведінки, а не про пряму антидепресивну дію (Thomas etal., 2009). Загалом, хоча величина зазначених ефектів є помірною, дані досліджень підтверджують, що цілеспрямований вплив на холінергічну і глутаматергічну дисфункції при деменції може забезпечувати вторинні переваги для поліпшення настрою та поведінки.
Результати застосування новітніх хворобомодифікувальних методів ще більше висвітлюють складну взаємодію КФ та афекту при нейродегенеративних розладах. Препарати моноклональних антитіл проти β-амілоїду сприяють уповільненню ПКФ на ранніх стадіях ХА, але поточні дані досліджень не підтверджують зменшення симптомів депресії, а будь-який потенційний вплив на настрій залишається спекулятивним. Подібна невизначеність існує і щодо терапії, спрямованої на τ-протеїн (Harris etal., 2025).
Серед нефармакологічних підходів втручання, що орієнтовані на доглядальників та базуються на активності (наприклад, структуровані програми фізичних вправ), мають найбільші докази поліпшення настрою та зменшення загального нейропсихіатричного навантаження за деменції. Щодо методів когнітивної реабілітації та нейромодуляції, як-от повторювана транскраніальна магнітна стимуляція, з’являються нові, але менш послідовні докази, переважно за депресії пізнього віку або порушень КФ на ранніх стадіях, а не при підтвердженій деменції (Silva etal., 2023). Втручання, що поліпшують настрій і КФ, також можуть мати подальші переваги щодо функціонування і рухливості, як-от впевнений контроль ходи, мобільність та активність у повсякденному житті, що підвищує їхню клінічну значущість для осіб літнього віку. Загалом накопичені результати вказують на появу нової терапевтичної парадигми, згідно з якою втручання все частіше спрямовані на взаємопов’язані шляхи ПКФ та афективних порушень у пізньому віці. У таблиці 2 наведено дані щодо результатів застосування та доказовості різних терапевтичних підходів.
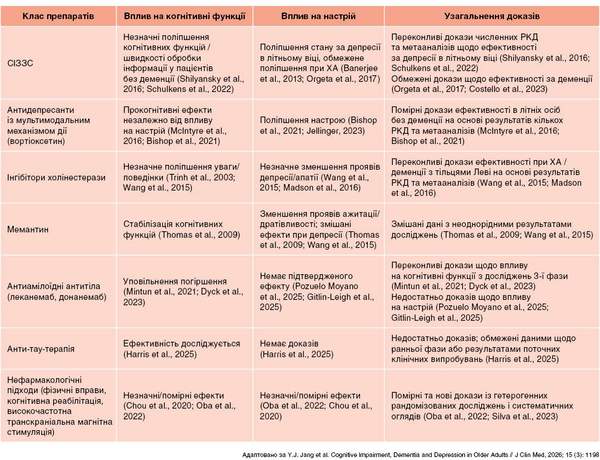
Висновки
вгоруДепресія та ПКФ у пізньому віці тісно взаємопов’язані, мають спільні клінічні прояви й частково перехресні нейробіологічні шляхи. Дані епідеміологічних, нейровізуалізаційних і біомаркерних досліджень свідчать, що депресія може бути як незалежним фактором ризику деменції, так і продромальним проявом нейродегенеративної/судинної патології. Водночас багато пацієнтів із деменцією мають симптоми депресії як частину ширшого спектра ППСД, а зміни настрою в них пов’язані з прискореним порушенням функціонування, більшим нейропсихіатричним навантаженням та погіршенням якості життя. Ці стадієзалежні зв’язки підкреслюють важливість виходу за межі бінарного розмежування «депресії» та «деменції» і прийняття інтегративної концептуальної основи їх динамічної двоспрямованої взаємодії. Для клінічної практики це означає поетапний підхід, у межах якого пізня депресія із когнітивними або судинними маркерами має спонукати до тривалого моніторингу, стратифікації ризику та своєчасного переходу до мультимодального втручання.
Взаємовплив терапевтичних підходів, спрямованих на настрій та КФ, зумовлює як можливості, так і обмеження. АД незначно поліпшують ВФ і ШОІ у літніх осіб без деменції, але за наявної деменції їх ефективність суттєво знижується. У пацієнтів із деменцією ІХЕ, мемантин та нефармакологічні втручання передусім зменшують прояви апатії та нейропсихіатричні симптоми, із менш послідовним впливом на симптоми депресії. Нові хворобомодифікувалні методи можуть змінити траєкторію розвитку ХА, але не підтверджено їхній прямий антидепресивний ефект. Y. J. Jang etal. (2026) наголошують на необхідності персоналізованих, стадіоспецифічних стратегій ведення пацієнтів, із тривалим моніторингом КФ, оцінюванням судинного та нейропсихіатричного ризику, мультимодальними втручаннями, адаптованими до їхніх клінічних профілів. За стійкого порушення ВФ, погіршення пам’яті, високого показника ГБР або швидкого порушення функціонування виправдане застосування нейровізуалізації або дослідження біомаркерів. Взаємодія настрою та КФ у пізньому віці чинить прямий вплив на функціонування, зокрема мобільність, стабільність ходи, ризик падінь і незалежність у повсякденній активності.
Підготувала Наталія Купко
Наш журнал
в соцсетях:
Мнения экспертов
Выпуски текущего года
Содержание выпуска 3 (168), 2026
-
Розширення ролі носимих медичних пристроїв у сучасній неврологічній практиці
-
Роль мистецтва в реабілітації та поліпшенні ментального здоров’я
-
Венлафаксин у терапії ПТСР: від доказової бази до вибору індивідуальної стратегії
-
Нові підходи, сміливі ідеї та найактуальніші теми у сфері неврології
-
Міастенія під маскою депресії та тривоги: клінічні пастки для психіатра і тактика ведення пацієнта
-
Нейропротекція та когнітивна реабілітація в сучасній психіатрії: фокус на комбіновану терапію
-
Антидепресант тразодон: фармакологічний профіль та мультимодальні й мультифункціональні ефекти
-
Рекомендації щодо ведення пацієнтів із нейропатичним болем унаслідок травми спинного мозку
Рассылка
Будьте в курсе последних обновлений – подпишитесь на рассылку материалов на Ваш e-mail
Подписаться








/thumbs/widget_nn26_3-168_titul.jpg)

/thumbs/widget_nn26_2-167_titul.jpg)
/thumbs/widget_nn26_1-166_titul.jpg)















